Психотропные средства – средства, регулирующие психические функции, прежде всего эмоции, мышление, память, мотивацию поведения. Препараты этой группы применяют для лечения психозов, депрессии, невротических состояний, а в некоторых случаях и у психически здоровых людей для уменьшения тревоги и эмоционального напряжения.
Для возникновения психической болезни, как и всякой другой, решающее значение имеют те внешние и внутренние условия, в которых действует причина. Причина вызывает болезнь не всегда, не фатально, а лишь при стечении ряда обстоятельств, причем для разных причин значение условий, определяющих их действие, различно. Возникновение психических болезней, их развитие, течение и исход зависят от взаимодействия причины, различных вредных влияний окружающей среды и состояния организма, т.е. от соотношения внешних (экзогенных) и внутренних (эндогенных) факторов.
Классификация психотропных средств
- Седативные средства
- Анксиолитики (транквилизаторы)
- Нейролептики (антипсихотические)
- Антидепрессанты
- Антиманиакальные (нормотимики)
- Психостимуляторы
- Ноотропы
Седативные средства
Седативные средства (от лат. sedatio — успокоение) – средства, усиливающие процессы торможения и/или ослабляющие процессы возбуждения в коре головного мозга.
Нормальное течение психических процессов обусловлено равновесием между возбудительными и тормозными процессами в ЦНС, а также достаточной для адекватного реагирования на внешние раздражители лабильностью. При наличии чрезмерных внешних раздражителей возможен срыв нервной деятельности, сопровождающийся преобладанием возбудительных процессов в ЦНС. В таких ситуациях показано назначение седативных средств. Седативные средства назначают, как правило, психически здоровым людям при повышенной эмоциональной лабильности, раздражительности.
Классификация седативных средств
- Малые дозы барбитуратов
- Бромиды (натрия бромид, калия бромид)
- Препараты растительного происхождения (препараты валерианы, пустырника, пассифлоры, пиона, хмеля обыкновенного и др.)
- Комбинированные средства (валокордин, новопассит, броменвал и др.)
Механизм действия седативных средств связывают с неизбирательным общеугнетающим влиянием на функцию ЦНС. Развитие седативного эффекта связывают либо с уменьшением процессов возбуждения, либо с усилением процессов торможения в головном мозге. Детально механизм действия препаратов этой группы не выяснен.
Анализ ассортимента седативных средств растительного происхождения
... спроса. При оценке степени удовлетворения спроса на препараты исследуемого ассортимента установлено, что у 48% седативных средств растительного происхождения спрос превышает предложение (валокордин, ... в аптеках Основными факторами, влияющими на потребление седативных средств растительного происхождения, являются: эффективность и безопасность препаратов, рекомендация врача и (или) провизора, цена, ...
Фенобарбитал (производное барбитуровой кислоты) оказывает седативное действие в дозе 1/5 от снотворной. В качестве монотерапии не используется. Входит в состав комбинированных седативных средств (корвалол, валокордин).
Бромиды (калия бромид и натрия бромид) обладают умеренным седативным действием, хорошо всасываются в ЖКТ, выводятся преимущественно почками. В токсических дозах соли брома вызывают сон и кому. Бромиды при длительном применении кумулируют в организме. Побочные эффекты могут проявляться комплексом патологических реакций, называемых бромизмом. Симптомы бромизма: сонливость, ослабление памяти, дрожание рук, век, языка, расстройство речи, запор, конъюнктивит, насморк, угреподобная сыпь на коже (бромодерма).
Препараты растительного происхождения более безопасны в применении, практически не вызывают серьезных побочных эффектов. Используются в разных лекарственных формах (настои, настойки, экстракты).
Являются средствами безрецептурного отпуска, что позволяет работнику первого стола рекомендовать их применение в определенных ситуациях. Вещества растительного происхождения комбинируют между собой (новопассит) или с другими группами седативных средств (валокордин, броменвал).
Основными фармакологическими эффектами являются седативный и потенцирующий (усиление действия средств, угнетающих ЦНС), что следует учитывать при одновременном применении с другими лекарственными средствами. Применяются седативные средства при повышенной нервной возбудимости, раздражительности, эмоциональной лабильности, легких формах бессонницы. Сравнивать клиническую эффективность седативных средств довольно сложно в связи с тем, что на оценку препарата влияет не только состав, но и субъективная оценка пациентом эффекта употребляемого средства. Как правило, у лиц с более слабым типом нервной системы эффект седативных средств проявляется более ярко.
При использовании седативных средств, особенно растительного происхождения, возможны аллергические реакции, большие дозы седативных средств вызывают сонливость. При длительном использовании бромидов возможна кумуляция.
Анксиолитики
Анксиолитики (от лат. anxius – тревожный, находящийся в страхе, и lysis – растворение, устранение), или транквилизаторы (от лат. tranquillare – спокойствие) – лекарственные средства, устраняющие тревогу, чувство страха, эмоциональное напряжение.
Тревогу оценивают как наиболее частую эмоциональную реакцию. Она может быть чертой личности, эмоциональным компонентом стресса и соматической патологии, симптомом в структуре расстройств личности. Тревога, возникающая как ответ на неопределенную или угрожающую ситуацию, а также на дефицит информации, является нормальной приспособительной реакцией, мобилизующей организм при реальной угрозе или трудном положении. Если выраженность тревоги чрезмерна по отношению к вызвавшей ее ситуации, или она вообще не обусловлена внешними факторами, диагностируют патологическую тревогу. У тревожных людей и при невротических состояниях снижена активность ГАМК-ергической тормозящей системы головного мозга, снижена плотность или наблюдается модификация бензодиазепиновых рецепторов.
107)Расстройства сферы ощущений и психосенсорного синтеза. Разграничение ...
... и токсоманиях, при шизофрении, при органичкских заболеваниях. 90) Психосенсорные расстройства. (метаморфопсии). Расстройства схемы тела. Клиника. Диагностическое значение. Метаморфопсии – искажение пространственных ... вызывает одновременно ответ с другого или нескольких анализаторов. Это продуктивные расстройства- свидетельствуют о психической патологии. Критерии диагностики 1. отсутствие качественной ...
Невротические расстройства (неврозы) – группа психогенно обусловленных болезненных состояний, характеризующихся многообразием клинических проявлений, не изменяющих самосознания личности и осознания болезни. Проявления невротических расстройств очень разнообразны: фобии, приступы тревоги (паники), навязчивые состояния, повышенная психическая и умственная утомляемость и пр.
Фобии (навязчивые страхи) — группа расстройств, при которых единственным или преобладающим симптомом является боязнь определенных ситуаций, не представляющих текущей опасности. Например, агорафобия — боязнь открытых пространств, клаустрофобия – боязнь закрытых помещений, канцерофобия – боязнь заболеть раком и пр.
Характерной панических чертой расстройств являются рецидивирующие приступы резко выраженной тревоги (паники), которые не ограничены какой-либо особой ситуацией или комплексом обстоятельств и, следовательно, непредсказуемы. Основная симптоматика включает внезапное возникновение сердцебиений, боли за грудиной, ощущения удушья, тошноту. Кроме того, как вторичное явление часто присутствует боязнь умереть, потерять контроль над собой или сойти с ума.
Особенностью навязчивых состояний является наличие повторяющихся навязчивых мыслей и действий. Навязчивые явления непреодолимы и возникают вопреки желанию больного.
При неврастении на первое место выходит чрезмерная психическая и/или физическая утомляемость, сопровождаемая головокружением, головной болью, беспокойством по поводу снижения своих умственных и физических способностей, раздражительностью.
На современном уровне знаний широкое распространение получила синдромальная классификация неврозов, которая нашла отражение в МКБ-10. Примеры формулировки диагноза:
Паническое расстройство (эпизодическая пароксизмальная тревожность).
Генерализованное тревожное расстройство.
Агорафобия.
Преимущественно навязчивые мысли или размышления.
Неврастения.
В структуре всех невротических расстройств присутствует повышенная тревожность. Основной группой средств, применяемой при неврозах, являются анксиолитики.
Классификация анксиолитиков
- Агонисты бензодиазепиновых рецепторов
1.1. с выраженным седативным и снотворным действием: диазепам, феназепам;
1.2. с минимальным седативным и снотворным действием («дневные» анксиолитики): медазепам, тофизопам и др.
- Агонисты серотониновых рецепторов: буспирон
- Антагонисты центральных H1-гистаминовых и М-холинорецепторов: гидроксизин
Фармакокинетика
Транквилизаторы -анксиолитики
... Глутаматергические анксиолитики Антагонисты NMDA-рецепторов (кетамин, фенциклидин, циклазоцин), антагонисты АМРА-рецептора (ифенпродил), ... на агонисты бензодиазепиновых рецепторов (диазепам, феназепам и др.), агонисты серотониновых рецепторов (буспирон) и препараты разного ... и минимально выражены седативный, снотворный, миорелаксантный эффекты — мезапам (рудотель), триоксазин, тофизопам ...
После перорального приёма анксиолитики быстро и полностью всасываются через желудочно-кишечный тракт, их биодоступность около 90%. Максимальную концентрацию в крови достигается в течение 1–2 ч. Большая часть введённого анксиолитика связывается с белками крови. Подавляющее большинство препаратов этой группы метаболизируется в печени (преимущественно с участием цитохрома Р450 3А4) и выводятся из организма в метаболизированном виде с мочой. Практически все анксиолитики хорошо проникают через гематоэнцефалический и плацентарный барьеры.
Механизмы действия анксиолитиков
Анксиолитики бензодиазепинового ряда взаимодействуют со специфическими бензодиазепиновыми рецепторами (являются агонистами этих рецепторов), входящими в состав постсинаптического ГАМКА-рецепторного комплекса в ЦНС. Бензодиазепины повышают чувствительность ГАМК-рецепторов к медиатору (ГАМК), что обусловливает повышение частоты открытия в цитоплазматической мембране нейронов каналов для входящих токов ионов хлора. В результате происходит усиление тормозного влияния ГАМК и угнетение межнейронной передачи в соответствующих отделах ЦНС.
Буспирон отличает от других анксиолитиков как химическая структура, так и механизм действия. Буспирон имеет сильный аффинитет к серотонинергическим 5-НТ1А-рецепторам и не имеет значимого аффинитета к ГАМК-ергической системе, включая бензодиазепиновые рецепторы. У препарата обнаружен умеренный аффинитет к D2-дофаминовым рецепторам.
Седативный и отчасти анксиолитический эффекты могут быть достигнут при блокировании центральных гистаминовых (Н1) рецепторов, так как гистаминергические структуры мозга регулируют многие фундаментальные процессы, в том числе цикл «сон–бодрствование», уровень бодрствования и уровень агрессивности, пищевое поведение, а также состояние когнитивных функций. Блокада гистаминовых рецепторов гидроксизином снижает уровень бодрствования, что приводит к снижению уровня тревожности.
Фармакологические эффекты и показания к применению
Эталонным представителей группы бензодиазепинов является диазепам. Он обладает выраженным анксиолитическим, седативным, снотворным действием. Кроме того, для него характерны миорелаксирующий, противосудорожный и потенцирующий эффекты. Применяют диазепам при невротических расстройствах, бессоннице, локальных спазмах скелетной мускулатуры. Диазепам является универсальным противосудорожным средством. Используется как средство премедикации.
Как правило, диазепам назначают внутрь. Начальная суточная доза составляет 0,005-0,01, при необходимости ее постепенно повышают. Для достижения быстрого анксиолитического, выраженного седативного эффектов, купирования судорог диазепам вводится парентерально (внутривенно, внутримышечно).
Внутривенное введение диазепама нельзя необходимо осуществлять медленно, контролируя функцию дыхания из-за возможного угнетения дыхательного центра.
«Дневные» анксиолитики оказывают преимущественно противотревожное действие с активирующим компонентом, улучшая психические функции, устраняя сковывающее влияние страха, тревоги, неуверенности в себе. Седативный, снотворный, миорелаксирующий эффекты выражены минимально. «Дневные» анксиолитики в меньшей степени нарушают умственную и физическую работоспособность, внимание, психомоторные реакции. Дозы подбирают индивидуально, начиная с минимальных: медазепам 0,005/сут, тофизопам 0,05-0,1/сут
При использовании анксиолитиков отмечается сонливость, атаксия, нарушение координации движений, снижение памяти и внимания. Эти феномены обусловлены седативным и миорелаксирующим действием препаратов и их объединяют термином «поведенческая токсичность». У большинства больных эти эффекты дозозависимы, со временем к ним происходит адаптация, поэтому наиболее ярко они проявляются у больных, впервые получающих препарат. У больных пожилого возраста побочные эффекты анксиолитиков проявляются чаще и при меньших дозах. Анксиолитики не рекомендуют назначать в качестве снотворных средств лицам любого возраста с синдромом ночного апноэ из-за опасности остановки дыхания во сне.
Применение анксиолитиков бензодиазепинового ряда может приводить к формированию лекарственной зависимости (психической и/или физической).
Риск возникновения зависимости возрастает при длительном применении, особенно в высоких дозах, а также у пациентов с лекарственной и алкогольной зависимостью в анамнезе. Лечение анксиолитиками может проводиться только под наблюдением врача. Курс лечения должен быть как можно более коротким. После прекращения приема препарата у пациента может возникнуть синдром отмены (тревога, депрессия, бессонница, тошнота, тремор).
Для предупреждения этого дозу препарата следует снижать постепенно. Согласительная комиссия ВОЗ (1996) не рекомендует применять препараты бензодиазепинового ряда непрерывно более 2–3 недель.
К анксиолитиками небензодиазепинового ряда относят буспирон и гидроксизин. Буспирон является агонистом серотониновых рецепторов. На бензодиазепиновые рецепторы не влияет и вследствие этого не оказывает стимулирующего эффекта на ГАМК-ергическую систему. Препарат не оказывает седативного действия, не обладает миорелаксирующим и противосудорожным эффектами. Анксиолитический эффект наступает позднее по сравнению с бензодиазепинами. Рекомендуемая начальная доза 0,005 3 раза в сутки.
Гидроксизин является антагонистом центральных H1-гистаминовых и М-холинорецепторов. Обладает выраженным седативным и умеренным анксиолитическим действием. В отличие от бензодиазепинов, при длительном применении гидроксизин не вызывает зависимости. Холиноблокирующее действие может проявляться сухостью во рту, задержкой мочеиспускания, запорами. Лечение начинают с дозы 0,025-0,5/сут.
Антипсихотические средства (нейролептики)
Антипсихотические средства (нейролептики) – лекарственные средства, способные устранять симптоматику психозов.
Психоз – это обобщенное название класса психических расстройств, общей чертой которого является нарушение процесса отражения объективной действительности, т.е. окружающий мир воспринимается искаженно. Психотические состояния сопровождаются продуктивной психопатологической симптоматикой – расстройствами мышления и восприятия. Расстройства мышления проявляются бредом (бред отношения, ревности, воздействия и пр.), расстройства восприятия – галлюцинациями (слуховыми, зрительными, тактильными).
При психотическом расстройстве наряду с позитивными (продуктивными) симптомами присутствуют негативные (дефицитарные) симптомы, включающие эмоциональную индифферентность, бедность речи, ангедонию и асоциальность. Эмоциональная индифферентность проявляется в неадекватной оценке явлений: например, событие которое заставляет нормального человека плакать, не вызывает у больного шизофренией никакой реакции. Ангедонией называется снижение способности испытывать удовольствие. Больной бесцельно проводит время и его не волнуют прежние увлечения. Асоциальность проявляется отсутствием интереса к общению с людьми.
Существуют различные теории развития психозов. Считают, что нарушение психической деятельности связано с изменениями основных медиаторных систем в соответствующих структурах мозга (ретикулярной формации, лимбической системе, гипоталамусе).
Так, психопродуктивная симптомтика (бред, галлюцинации) возникает при гиперфункции дофаминовых систем. Психоэмоциональное напряжение, тревога, страх, связаны с повышением роли адренергических, серотонинергических систем.
В зависимости от причин возникновения принято подразделять психозы на эндогенные (вызванные внутренними факторами, при этом может отсутствовать органическое поражение головного мозга) и экзогенные (возникшие под влиянием внешних факторов).
Такое деление достаточно условно, т.к. психоз может начаться в результате воздействия внешних факторов (например, приема наркотиков), но затем заболевание будет развиваться уже за счет внутренних факторов (при наличии предрасположенности к развитию психических нарушений, которая не проявляла себя до определенного момента).
К типичным эндогенным психозам относят шизофрению, шизоаффективные психозы, маниакально-депрессивный психоз (биполярное расстройство психотического уровня).
Экзогенные психозы представлены реактивными или ситуационными психозами, возникшими в ответ на сильную психотравмирующую ситуацию (смерть близкого человека, насилие).
Также в клинике психозов достаточно широко представлены инфекционные психозы (последствие менингита, энцефалита), интоксикационные психозы (в результате приема наркотиков и алкоголя).
Примеры формулировки диагноза:
Параноидная шизофрения.
Острое полиморфное психотическое расстройство без симптомов шизофрении.
Шизоаффективное расстройство, маниакальный тип.
Биполярное аффективное расстройство, текущий эпизод мании с психотическими симптомами.
Нейролептики, обладая способностью вмешиваться в обмен определенных медиаторных структур мозга, уравновешивают медиаторный фон. Проникая в головной мозг, они блокируют дофаминовые, адренергические, серотонинергические, холинергические рецепторы, либо тормозят выброс соответствующих медиаторов, а также могут инактивировать их в нервном окончании.
Классификация антипсихотических средств
- Производные фенотиазина: хлорпромазин, трифлуоперазин
- Производные бутирофенона: галоперидол, дроперидол
- Производные тиоксантена: хлорпротиксен
- Производные дибензодиазепина: клозапин, оланзапин
- Замещенные бензамиды: кветиапин
- Производные пиримидина: рисперидон
С клинической точки зрения больший интерес представляет следующая классификация:
- Типичные нейролептики
Психоседативные: хлорпромазин, дроперидол, хлорпротиксен
Антипсихотические: трифлуоперазин, галоперидол
- Атипичные нейролептики: клозапин, оланзапин, кветиапин, рисперидон
Фармакокинетика
Как все средства, обладающие значимой ЦНС активность, антипсихотики выражено липофильны. Их биодоступность при приёме внутрь колеблется от 30 до 80%. Парентеральное введение значительно повышает их биодоступность. Способность антипсихотическмх средств влиять на периферические дофаминовые и холинергические рецепторы может значимо менять моторику желудочно-кишечного тракта, нарушая при этом всасывание препаратов. Антипсихотики проявляют высокое сродство к белкам плазмы, что может означать клинически значимое изменение в их концентрации в плазме при использовании препаратов, конкурентно связывающихся с белками. Благодаря высокой липофильности антипсихотики накапливаются в тканях мозга, лёгких и других органах в концентрациях значительно более высоких, чем в плазме крови. Так, содержание хлорпромазина в мозге в 4–5 раз выше, чем в плазме, галоперидола – в 10 раз, а клозапина – в 12–50 раз превышает его концентрацию в плазме крови. Концентрация антипсихотика в плазме не имеет связи с формированием собственно антипсихотического эффекта.
Скорость метаболизма и объём распределения препаратов зависят от различных факторов: возраст, курение, пол, масса тела, диета, раса, лекарственный анамнез.
Антипсихотики подвергаются активной биотрансформации, которая происходит не только в печени, но и в лёгких, мозге, почках и кишечнике.
Механизм действия и фармакологические эффекты
Антипсихотическое действие нейролептиков связано с блокадой дофаминовых D2-рецепторов мезолимбической и мезокортикальной систем. Нейролептики имеют сходство структуры с дофамином и по конкурентному принципу блокируют рецепторы дофамина. С блокадой этих рецепторов связывают устранение позитивной симптоматики психозов (бреда, галлюцинаций).
Блокадой рецепторов серотонина (5-НТ2А) обусловлено ослабление негативной симптоматики. Для реализации антипсихотического действия требуется длительное время (дни, недели, месяцы).
Психоседативное (глубочайшее седативное, нейролептическое) действие связывают с блокадой центральных Н1-рецепторов гистамина и ?–адренорецепторов. Этот эффект развивается непосредственно после введения препарата.
Гипоталамо-гипофизарная система: нейролептики угнетают центр терморегуляции, блокируя его ?–адренорецепторы, повышают секрецию пролактина, являясь антагонистами D2-рецепторов дофамина в аденогипофизе.
Реализация противорвотного действия обусловлена блокадой D2-рецепторы дофамина в триггерной зоне рвотного центра.
С блокадой D2-рецепторов дофамина в базальных ядрах (хвостатом ядре, скорлупе, бледном шаре) связан основной побочный эффект — экстрапирамидные расстройства (лекарственный паркинсонизм).
Антипсихотические средства, блокируя ?–адренорецепторы сосудов, способны снижать артериальное давление.
Эффекты блокады М-холинорецепторов. Антагонизм с центральными М-холинорецепторами нивелирует экстрапирамидные расстройства, но может сопровождаться ухудшением когнитивных функций. Центральные М-холиноблокаторы (тригексифенидил) используются для коррекции экстрапирамидных расстройств. Периферическое М-холиноблокирующее влияние проявляется нарушением аккомодации, тахикардией, сухостью во рту, запорами, задержкой мочеиспускания.
Аффинитет к указанным типам рецепторов и, соответственно, степень выраженности тех или иных эффектов у антипсихотических средств различна.
Сравнительная характеристика антипсихотических средств
|
Препарат |
Блокада рецепторов* |
Антипсихоти-ческое действие |
Психоседативное действие |
Экстрапирамид-ные расстройства |
|
Психоседативные нейролептики |
||||
|
Хлорпромазин |
D2, , 5-НТ2А, М, Н1 |
++ |
++++ |
++ |
|
Дроперидол |
D2, , 5-НТ2А |
++ |
++++ |
+ |
|
Хлорпротиксен |
D1, D2, , 5-НТ2А, М
|
++ |
+++ |
+ |
|
Антипсихотические нейролептики |
||||
|
Галоперидол |
D2, 5-НТ2А |
+++ |
++ |
+++ |
|
Трифлуоперазин
|
D2, , 5-НТ2А |
+++ |
++ |
+++ |
|
Атипичные нейролептики |
||||
|
Клозапин |
D4, , 5-НТ2А, 5-НТ2С, М, Н1 |
+++ |
++++ |
|
|
Оланзапин |
D4, , 5-НТ2А, М, Н1
|
+++ |
+ |
|
|
Кветиапин |
D4, 5-НТ2А, Н1 |
+++ |
+ |
+ |
|
Рисперидон |
D2, D3, D4, , 5-НТ2А, Н1
|
+++ |
++ |
+ |
Примечание. * – D2-рецепторы дофамина, –адренорецепторы, 5-НТ2А-рецепторы серотонина, М-холинорецепторы, Н1-рецепторы гистамина.
Психоседативные нейролептики
Оказывают сильное психоседативное влияние и только умеренный антипсихотический эффект. Купируют галлюцинаторно-бредовое или маниакальное возбуждение. Возникающие экстрапирамидные расстройства (лекарственный паркинсонизм) протекают более легко, чем при применении антипсихотических нейролептиков.
Хлорпромазин оказывает выраженное психоседативное действие. Антипсихотический эффект средней силы, развивается к 4-7 дню лечения. В значительной степени угнетает центр терморегуляции. Потенцирует действие средств для наркоза, снотворных средств, анальгетиков. Применяют для лечения острых и хронических психозов, купирования психомоторного возбуждения. Используют для создания управляемой гипотермии (для повышения устойчивости тканей к гипоксии при операциях с экстракорпоральным кровообращением), как противорвотное средство на фоне лучевой и химиотерапии. На фоне лечения возникают вялость, сонливость, ощущение полного безразличия, моторная заторможенность. В первые дни лечения вызывает ортостатическую гипотензию. Обладает выраженными холиноблокирующими свойствами.
Дроперидол оказывает кратковременное психоседативное, потенцирующее, гипотензивное действие. Используют в форме раствора для парентерального введения. Применяют для премедикации, купирования острого психомоторного возбуждения, гипертонического криза. В сочетании с опиоидным анальгетиком фентанилом используют для нейролептанальгезии.
Хлорпротиксен уступает хлорпромазину по выраженности психоседативного и антипсихотического эффектов. Особенностью является наличие антидепрессивной активности. В обычных дозах фактически не вызывает экстрапирамидных расстройств.
Антипсихотические нейролептики
Препараты этой группы оказывают сильное антипсихотическое действие и слабый или умеренный психоседативный эффект. Такое действие называют инцизивным («режущим»).
При курсовом применении в малых дозах повышают активность больных, восстанавливают мотивации, увеличивают моторную активность. Показаны для длительной терапии психических заболеваний, особенно если они протекают с явлениями заторможенности. Паркинсонизм и другие нарушения в двигательной сфере протекают в более тяжелой форме, чем при применении психоседативных нейролептиков.
Галоперидол оказывает выраженное антипсихотическое действие, которое сочетается с умеренным седативным и выраженным противорвотным эффектами. Часто вызывает экстрапирамидные расстройства, практически не оказывает холиноблокирующего действия.
Трифлуоперазин является одним из наиболее активных антипсихотических средств с активирующим эффектом. Оказывает выраженное действие на продуктивную симптоматику психозов. В сравнении с хлорпромазином оказывает более слабый гипотензивный, холиноблокирующий, седативный эффекты. Оказывает выраженное противорвотное действие и кроме использования в качестве антипсихотического средства применяется как противорвотное при лучевой болезни.
Атипичные нейролептики
Атипичные антипсихотические средства в отличие от типичных гораздо реже и в меньшей степени вызывают экстрапирамидные расстройства и нейроэндокринные нарушения, связанные с блокадой D2-рецепторов. Отсутствие у атипичных нейролептиков значительных экстрапирамидных расстройств обусловлено высокими значениями соотношения блокады 5-НТ2А / D2-рецепторов. Атипичные нейролептики блокируют D2-рецепторы дофамина в меньшей степени и на непродолжительный срок по сравнению с типичными. Высокая степень блокады рецепторов серотонина (5-НТ2А) уменьшает выраженность побочных эффектов (экстрапирамидных расстройств, гиперпролактинемии), свойственных типичным нейролептикам.
Клозапин преимущественно блокирует дофаминовые D4-рецепторы и серотониновые 5-НТ2А-рецепторы, а также Н1-рецепторы гистамина, ?–адренорецепторы и М-холинорецепторы. Проявляет антипсихотическую, психоседативную активность, устраняет негативную симптоматику, не вызывает заторможенности. При терапии клозапином не повышается секреция пролактина, редко возникают экстрапирамидные расстройства. К побочным эффектам относятся артериальная гипотензия, атропиноподобные эффекты, повышение аппетита и массы тела. Наиболее серьезным побочным эффектом является гранулоцитопения (вплоть до агранулоцитоза), вследствие чего лечение следует проводить под контролем состава периферической крови.
Оланзапин в сравнении с клозапином обладает меньшим психоседативным влиянием и в меньшей степени влияет на картину крови.
Кветиапин проявляет более высокое сродство к рецепторам серотонина (5-НТ2), чем к рецепторам дофамина D1 и D2 в головном мозге. Не обладает холиноблокирующими свойствами.
Рисперидон обладает высокой аффинностью к серотонин- и дофаминергическим рецепторам. Практически не влияет на М-холинорецепторы. Возможно, вследствие этого он чаще, чем другие атипичные нейролептики вызывает экстрапирамидные расстройства.
Антидепрессанты
Антидепрессанты – лекарственные средства, применяемые для лечения депрессий.
Депрессия – психическое расстройство, характеризующееся патологически сниженным настроением (гипотимией) с негативной, пессимистической оценкой себя, своего положения в окружающей действительности и своего будущего. Оно выражается по-разному – от чувства скуки и грусти до ангедонии (снижения способности испытывать удовольствие), ощущения безысходности, социального и психологического тупика. У больных появляется пессимизм в оценке своих способностей, мысли о собственной неполноценности и никчемности, идея вины перед окружающими. Депрессия серьезно влияет на качество жизни и адаптационные возможности человека. Депрессия, как ни одно психическое заболевание, сопряжена с риском самоубийства – самого трагического исхода, приводящего к преждевременной смерти. Для общества это означает потерю его членов в самом продуктивном периоде их жизни (основная доля связанных с депрессией самоубийств приходится на возраст от 15 до 34 лет).
Наиболее разработана биохимическая теория возникновения депрессий. Многообразие клинических проявлений депрессивных расстройств свидетельствует об участии в патогенезе депрессии взаимосвязанных нарушений ряда нейрохимических систем. В настоящее время считается общепринятым и наиболее обоснованным, что ключевые патогенетические механизмы депрессии связаны с функциональным дефицитом серотонинергической системы и со сложной дисрегуляцией норадренергической системы. Согласно этой теории при депрессии отмечается патологически сниженное содержание моноаминов норадреналина и серотонина в головном мозге, а также снижается чувствительность соответствующих рецепторов.
Антидепрессанты способны повысить настроение и снизить уровень тревоги только у лиц с клинически выраженными признаками депрессивного расстройства. У здоровых людей большинство антидепрессантов не вызывает подъём настроения, но напротив, приводят к заторможенности и сонливости. При переживании тягостных эмоций здоровыми людьми они практически неэффективны.
Классификация антидепрессантов
- Ингибиторы обратного нейронального захвата моноаминов
1.1. неселективные: амитриптилин, имипрамин;
1.2. селективные:
ингибиторы обратного захвата серотонина (СИОЗС): флуоксетин, пароксетин, циталопрам;
ингибиторы обратного захвата норадреналина (СИОЗН): мапротилин;
ингибиторы обратного захвата серотонина и норадреналина (СИОЗСН) или препараты двойного действия: венлафаксин, дулоксетин.
- Ингибиторы моноаминоксидазы (МАО)
2.1. неселективные (МАО-А и МАО-В): ниаламид;
2.2. селективные (МАО-А): моклобемид.
- «Атипичные» антидепрессанты (с недостаточно известным механизмом действия): тианептин, адеметионин.
Фармакокинетика
Большинство антидепрессантов относительно хорошо всасывается в желудочно-кишечном тракте при приёме внутрь. Их биодоступность сильно варьирует. Связывание антидепрессантов с белками крови колеблется от 80% до 98%. Вследствие такого значительного связывания с белками сочетание их с другими препаратами, которые тоже имеют высокую степень связывания, может привести к конкурентному вытеснению антидепрессантов и увеличению их свободной фракции или, наоборот, к вытеснению сопутствующего препарата и увеличению его концентрации в крови, что может быть причиной побочных эффектов. Все антидепрессанты хорошо проникают через гистогематические барьеры, в том числе через гематоэнцефалический и плацентарный, поэтому использование их в период беременности крайне нежелательно. Большинство антидепрессантов подвергаются значительной биотрансформации. Расщепление препаратов осуществляется системой цитохрома Р450 Совместное применение антидепрессантов и других средств, которые также метаболизируются этими цитохромами или имеют влияние на их активность, может привести к существенному изменению фармакокинетических показателей антидепрессантов. Антидепрессанты выводятся из организма преимущественно почками, в основном, в виде метаболитов, небольшая часть выводится с желчью, а также выделяется с грудным молоком.
Механизм действия
Серотонин называют нейромедиатором «хорошего настроения», так как он регулирует импульсивные влечения, половое поведение и смену циклов сна, облегчает засыпание, снижает агрессивность, восприятие боли. Норадреналин участвует в поддержании бодрствования и необходим для формирования когнитивных адаптационных реакций.
Антидепрессанты оказывают свое терапевтическое влияние путем потенцирования синаптической передачи в серотонинергических и адренергических синапсах за счет увеличения концентрации и продолжительности «жизни» нейротрансмиттера в синаптической щели. При этом одни препараты ингибируют моноаминксидазу (МАО) – фермент, обеспечивающий метаболизм моноаминов в синаптической щели, а другие подавляют их обратный захват пресинаптическими структурами.
Точки приложения эффекта антидепрессантов разных групп
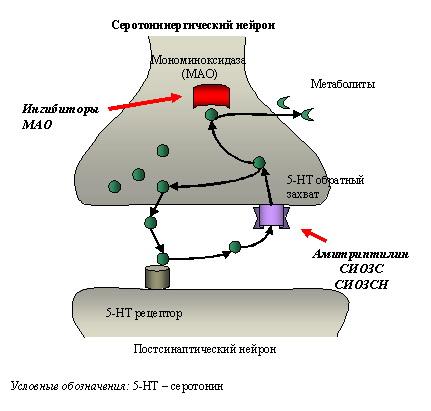
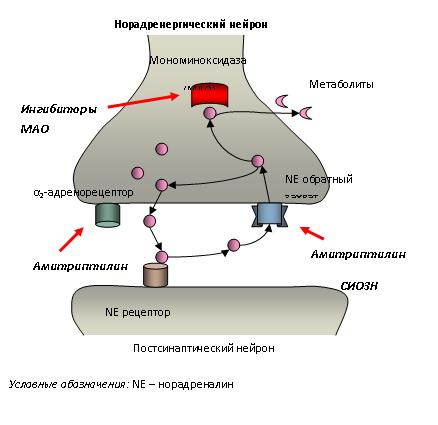
Основные фармакологические эффекты
Антидепрессанты оказывают тимоаналептическое действие (греч. thymos – душа, настроение, ana – приставка, означающая движение вверх, lepticos – способный воспринимать).
У больных депрессией появляется хорошее ровное настроение, возвращаются оптимизм, жизненные цели, исчезают чувство безнадежности и суицидальные мысли. Тимоаналептическое действие наступает через 10-15 дней постоянного приема антидепрессанта.
Помимо тимоаналептического действия антидепрессант может обладать психостимулирующим или седативным действием. Если этого нет, говорят о сбалансированном действии антидепрессанта.
Некоторые антидепрессанты наряду с ингибированием нейронального захвата моноаминов в различной степени блокируют М-холинорецепторы, рецепторы гистамина Н1, адренорецепторы. Это с одной стороны обеспечивает дополнительный противотревожный и седативный эффекты, а с другой – реализацию побочного действия препаратов.
Неселективные ингибиторы обратного захвата моноаминов
Амитриптилин неизбирательно блокирует обратный нейрональный захват серотонина и норадреналина, увеличивая содержание этих моноаминов в синаптической щели. Тимоаналептическое действие сочетается с выраженном седативным эффектом, обусловленным блокадой центральных Н1-рецепторов гистамина, М-холинорецепторов и пресинаптических ?2–адренорецепторов. Амитриптилин используют при депрессиях, сопровождающихся тревогой, ажитацией. Препарат также обладает анальгезирующим действием. В развитии анальгезии участвует серотонинергическая и адренергическая антиноцицептивная система. В связи с этим амитриптилин используют при хронических болевых синдромах, сопровождаемых депрессией. Блокируя ?–адренорецепторы сосудов, амитриптилин способен снижать артериальное давление. Периферическое М-холиноблокирующее влияние проявляется нарушением аккомодации, повышением внутриглазного давления, тахикардией, сухостью во рту, запорами, задержкой мочеиспускания. Для амитриптилина характерна высокая кардиотоксичность.
Имипрамин в отличие от амитриптилина оказывает тимоаналептический и стимулирующий эффекты. Наиболее эффективен при депрессии в сочетании с астенией. Его назначают в первой половине дня в связи с опасностью бессонницы. Холиноблокирующие свойства выражены в меньшей степени, чем у амитриптилина.
Селективные ингибиторы обратного захвата моноаминов
Препараты этой группы отличаются от неселективных ингибиторов обратного захвата моноаминов прежде всего меньшим (вплоть до полного отсутствия) холиноблокирующим действием, а также незначительным влиянием на ?–адрено- и гистаминовые рецепторы, что выгодно отличает их от препаратов неизбирательного действия, меньшим количеством побочных эффектов, связанных с блокадой этих рецепторов.
Пароксетин блокирует преимущественно обратный нейрональный захват серотонина, что приводит к усилению серотонинергических влияний в ЦНС. Тимоаналептическое действие при регулярном применении проявляется в среднем через 10-14 дней. На фоне лечения пароксетином наблюдается уменьшение тревоги, депрессии, нарушений сна. Препарат назначают 1 раз в сутки.
Флуоксетин по механизму действия близок к пароксетину. У него отсутствует седативный эффект, напротив, он оказывает некоторое психостимулирующее влияние. Применяют при депрессии, сопровождающейся заторможенностью, сонливостью. Тимоаналептический эффект проявляется через 2-3 недели, стимулирующее влияние – через 5-7 дней. Из побочных эффектов отмечается нарушение аппетита (анорексигенные свойства), нервозность, бессонница.
Мапротилин в большей степени подавляет обратный захват норадреналина пресинаптическими нервными окончаниями по сравнению с серотонином, что позволяет говорить об избирательном ингибировании мапротилином обратного нейронального захвата норадреналина. М-холиноблокирующая и ?–адреноблокирующая активность выражены умеренно. Антидепрессивное действие сочетается с анксиолитическим и седативным эффектами. Применяется мапротилин при депрессивных расстройствах, в том числе сопровождающихся тревогой, страхом, раздражительностью.
Венлафаксин и дулоксетин относят к препаратам двойного действия, они ингибируют обратный нейрональный захват и серотонина, и норадреналина. Одно из преимуществ антидепрессантов двойного действия – незначительное влияние на активность цитохромов печени, поэтому они достаточно безопасны при использовании в сложных лечебных схемах, особенно у больных с сопутствующими заболеваниями. о механизму действия близок к пароксетину. ение тревоги через 10-14 дней. ельного действия меньшим количеством побочных эффекто
Ингибиторы МАО
Известно два изофермента МАО: тип А осуществляет окислительное дезаминирование серотонина, норадреналина и адреналина, тип В инактивирует другие биогенные амины. МАО-А функционирует в нейронах, слизистой оболочке кишечника и печени. Изофермент пищеварительного тракта окисляет фенилаланин, тирозин и тирамин пищи. Активность МАО-В определяется исключительно в головном мозге. Антидепрессанты – ингибиторы МАО (ИМАО), уменьшая инактивацию серотонина и норадреналина, вызывают накопление этих нейромедиаторов.
В настоящее время применяют единственный неселективный ИМАО – ниаламид. Применяют для терапии депрессии с астеническим синдромом. Среди побочных эффектов наибольшую известность получил «сырный криз» (тираминовый синдром) – артериальная гипертензия, тахикардия, нарушение сердечного ритма, судороги при питании продуктами, богатыми тирамином (бананы, сыр, шоколад, печень).
В норме тирамин, поступающий с пищей, инактивируется под влиянием МАО кишечника и печени. При ингибировании МАО тирамин поступает в системный кровоток и действует как адреномиметик.
Современные антидепрессанты ингибируют МАО-А в головном мозге, не влияя на МАО-В и ферменты периферических тканей. Моклобемид избирательно и обратимо ингибирует фермент МАО-А, в результате чего временно подавляет метаболизм биогенных моноаминов серотонина и норадреналина. Обладает психостимулирующим влиянием. Оказывает М-холиноблокирующее действие, может усиливать прессорный эффект симпатомиметиков.
Тактика выбора антидепрессанта
Антидепрессанты подразделяются на препараты, предпочтительно применяемые в общемедицинской и специализированной психиатрической сети:
антидепрессанты первого ряда (применяемые в общемедицинской практике): флуоксетин, пароксетин, флувоксамин, циталопрам, венлафаксин, дулоксетин пр.;
антидепрессанты второго ряда (применяемые в специализированной психиатрической сети): амитриптилин, имипрамин, ниаламид и пр.
К средствам первого ряда относят современные антидепрессанты, сочетающие мягкий антидепрессивный эффект с хорошей переносимостью. Общие свойства препаратов первого ряда, обеспечивающие их успешное применение в общемедицинской практике:
достаточная выраженность антидепрессивного действия;
минимальная потребность в титрации дозы;
отсутствие тяжелых побочных эффектов;
минимум терапевтически значимых нежелательных взаимодействий с соматотропными средствами;
отсутствие такого значимого для качества жизни и самооценки больных депрессиями побочного эффекта, как увеличение массы тела.
Препараты второго ряда обладают высокой психотропной активностью. Трициклические антидепрессанты можно рассматривать как наиболее хорошо исследованные и надежные средства терапии тяжелых депрессий. Вместе с тем для средств второго ряда характерна значительная выраженность побочных эффектов, высокий риск взаимодействия с соматотропными средствами, что не позволяет считать эти средства безопасными для применения в общемедицинской практике.
Антиманиакальные средства
Антиманиакальные средства (нормотимики) – препараты, нормализующие настроение при мании и применяемые для предупреждения развития маниакальной и депрессивной симптоматики при маниакально-депрессивном психозе.
Маниакально-депрессивный психоз – биполярное расстройство, сопровождающееся чередованием фаз депрессии и мании со светлыми промежутками. Маниакальное состояние проявляется повышенной, но нецелесообразной, непроизводительной активностью, неадекватным энтузиазмом, патологической веселостью, чрезмерной физической активностью, ускорением движений и речи, быстрой сменой мыслей, идей.
В качестве антиманиакальных средств применяют соли лития, карбамазепин и вальпроевую кислоту.
Механизм действия солей лития до конца не выяснен. Считают, что ионы лития через быстрые натриевые каналы проникают в нейроны, накапливаются там и блокируют трансмембранный транспорт ионов натрия. В итоге нарушаются процессы деполяризации мембран нейронов. Лития карбонат применяется для лечения маниакальных состояний и профилактики рецидивов маниакально-депрессивного психоза. Эффект развивается медленно (через 2-3 недели постоянного применения), необходимо длительное применение. Характерные побочные эффекты: тремор, атаксия, нарушения координации, жажда, полиурия. Препарат обладает малой широтой терапевтического действия. Токсическое действие развивается при превышении терапевтической концентрации в 2-3 раза.
Карбамазепин и препараты вальпроевой кислоты применяют для лечения маниакальных состояний и профилактики рецидивов маниакально-депрессивного психоза в сочетании с солями лития при недостаточной эффективности последних.
Психостимуляторы
Психостимуляторы – лекарственные средства, повышающие умственную и физическую работоспособность, ускоряя темп деятельности.
Классификация психостимуляторов
- Фенилалкиламины: амфетамин, пиридитол
- Производные сиднонимина: мезокарб и др.
- Производные метилксантина: кофеин
Психостимуляторы уменьшают утомление и сонливость, отодвигают потребность во сне. После приема психостимуляторов возникают прилив сил, желание работать, улучшается настроение. Возможно появление тревоги, внутреннего напряжения. Психостимуляторы повышают двигательную активность, иногда вызывая моторную суетливость. Нарушают кинестезию (греч. kineo – двигать, aesthesis – ощущение, чувство) – контроль за предельно допустимой нагрузкой: человек, не чувствуя утомления, продолжает работу до изнеможения.
Психостимуляторы повышают краткосрочную память, улучшают показатели стереотипной, доведенной до автоматизма работы. При творческой работе, требующей анализа и решения сложных задач, увеличивают количество ошибок, вызывают снижение внимания. Таким образом, на фоне неглубокого утомления психостимуляторы мобилизуют функциональные и энергетические ресурсы, позволяя продолжить работу на короткий срок. При тяжелом утомлении они истощают организм. Эти средства используются коротким курсом или однократно.
Механизм действия амфетамина связывают со способностью вызывать высвобождение дофамина, норадреналина и серотонина и тормозить обратный нейрональный захват этих нейромедиаторов. Является сильным психостимулятором. Вызывает эйфорию, всплеск работоспособности, хотя точность выполнения работы снижается. Быстро наступает отрицательное последействие (истощение), требующее полноценного отдыха в течение нескольких дней. Вызывает тахикардию, повышение артериального давления, увеличение потребности миокарда в кислороде. Препарат кумулирует в организме, вызывает лекарственную зависимость. В настоящее время применение препарата ограничено. Входит в Список II Перечня наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в Российской Федерации (Постановление Правительства РФ от 30 июня 1998 г. № 681).
Мезокарб вызывает активацию норадренергических влияний в ЦНС, вытесняя медиатор норадреналин из везикул в синаптическую щель. Оказывает мягкое психостимулирующее действие без начальной эйфории и последующего истощения. Периферическое симпатомиметическое действие выражено незначительно. Лекарственная зависимость развивается медленнее, чем к производным фенилалкиламина. Применяют при умственном и физическом переутомлении, патологической сонливости (нарколепсии), астении после перенесенных заболеваний, интоксикаций. Назначают мезокарб в первой половине дня. Мезокарб может вызывать раздражительность, возбуждение, бессонницу, снижение аппетита, повышение артериального давления.
Кофеин оказывает сложное влияние на содержание внутриклеточного кальция, аденозиновые рецепторы и фосфодиэстеразу, разрушающую цАМФ. Кофеин ингибирует фосфодиэстеразу и таким образом повышает концентрацию цАМФ в тканях мозга, сердца и других органов. Кофеин оказывает психостимулирующее и аналептичесое действие (стимулирует дыхательный и сосудодвигательный центры продолговатого мозга).
Применяется при умственном и физическом переутомлении, патологической сонливости (нарколепсии), артериальной гипотензии, мигрени (в комбинации с алкалоидами спорыньи).
Кофеин может вызывать возбуждение ЦНС (раздражительность, бессонницу), тошноту, рвоту, тахикардию, аритмию. При длительном применении возможно развитие зависимости (теизм).
Ноотропные средства
Ноотропные средства — лекарственные средства, способные улучшать высшие интегративные функции головного мозга (память, внимание, интеллект), а также повышать устойчивость мозга к агрессивным воздействиям.
Термин ноотропные средства происходит от двух греческих слов noos – ум, разум, мышление и tropos – стремление. Таким образом, в названии отражена направленность действия препаратов этой группы на высшие интегративные функции головного мозга – интеллектуальные и мнестические.
Классификация лекарственных средств с ноотропным действием
- Производные пирролидона (рацетамы): пирацетам, фенотропил
- Холинергические ЛС: ривастигмин, лецитин и др.
- ГАМК-ергические ЛС: гамма-аминомасляная кислота, гопантеновая кислота, никотиноил-ГАМК, фенибут
- Глутаматергические ЛС: глицин
- Нейропептиды и их аналоги: актовегин, церебролизин
- Антиоксиданты и мембранопротекторы: милдронат
- Церебральные вазодилататоры: винпоцетин, ницерголин, нимодипин, пентоксифиллин, циннаризин,
Основным представителем группы является пирацетам. Пирацетам, производное пирролидона, является циклическим производным ГАМК. Ноотропное действие препарата связывают с улучшением метаболических процессов в нервный клетках. Пирацетам повышает синтез фосфолипидов и белка, активирует аденилатциклазу, повышает уровень АТФ. Препарат увеличивает утилизацию глюкозы в головном мозге, улучшает микроциркуляцию, не вызывая сосудорасширяющего действия. Нормализация энергетических процессов под влиянием пирацетама приводит к повышению устойчивости тканей мозга к гипоксии и интоксикациям. Препарат также обладает антигипоксическим и мембраностабилизирующим действием.
Пирацетам применяют при заболеваниях, сопровождающихся снижением памяти, внимания (атеросклероз сосудов мозга, ЧМТ), задержке умственного развития у детей, остром нарушении мозгового кровообращения, остром отравлении и хронической интоксикации алкоголем, наркотиками, снотворными.
На здоровых людей ноотропные средства существенного влияния не оказывают. В отличие от психостимуляторов, ноотропы не вызывают психомоторного возбуждения, истощения функциональных возможностей организма, лекарственной зависимости.
